Рекомендации
Клинические рекомендации по детской ревматологии
Рекомендации
Ассоциация детских ревматологов
10.06.2021
Рекомендации
Союз педиатров России
01.02.2018
Рекомендации
Союз педиатров России
03.04.2017
Рекомендации
Союз педиатров России
06.06.2016
Рекомендации
Союз педиатров России
04.02.2016
Рекомендации
Союз педиатров России
04.03.2016
Рекомендации
Союз педиатров России
03.03.2016
Новости
1 — 7 из 8
Начало | Пред. |
1
2
|
След. |
Конец
МЕДИЦИНСКИЙ КОНТЕНТ
Страница, которую вы собираетесь посмотреть, содержит медицинский контет. Пожалуйста, подтвердите, что вы
являетесь медицинским сотрудником.
МЕДИЦИНСКИЙ КОНТЕНТ
Эта страница содержит медицинский контент. Пожалуйста, подтвердите, что вы являетесь медицинским
сотрудником.
6.3. Острая ревматическая лихорадка
Острая ревматическая лихорадка (ОРЛ) — системное воспалительное заболевание соединительной ткани, возникающее у предрасположенных лиц после перенесенных тонзиллита или фарингита, которые вызваны БГСА. ОРЛ в подавляющем большинстве случаев развивается в детском возрасте — от 7 до 15 лет, реже у лиц более старших возрастных групп (МКБ-10, см. ).
Хроническая ревматическая болезнь сердца — заболевание сердца, возникающее после ОРЛ и характерное поражением сердечных клапанов в виде поствоспалительного краевого фиброза клапанных створок или формированием порока сердца.
Эпидемиология
В настоящее время ОРЛ и хроническая ревматическая болезнь сердца по-прежнему занимают особое место в структуре ревматической патологии и сохраняют большое влияние на формирование сердечно-сосудистых заболеваний. В 2005–2010 гг. первичная заболеваемость ОРЛ в Российской Федерации среди детей в возрасте до 14 лет составляла 3,02–1,99 на 100 тыс. детского населения, а среди подростков 15–17 лет — 4,8–2,7 на 100 тыс. В то же время частота регистрации хронической ревматической болезни сердца в указанных возрастных группах была значительно выше (29,3–19,0 и 64,5–47,5 на 100 тыс. соответственно).
Этиология
В развитии ОРЛ ведущая роль принадлежит высоковирулентным штаммам БГСА, вызывающим явления тонзиллита и фарингита. Высокую патогенность этих штаммов БГСА определяют высокой контагиозностью, тропностью к слизистой оболочке верхних дыхательных путей, индукцией типоспецифических АТ, наличием М-протеина (специфического белка, входящего в состав клеточной стенки стрептококка и подавляющего его фагоцитоз).
Патогенез
В патогенезе ОРЛ определяющим являются 2 процесса.
-
Прямое токсическое воздействие ферментов БГСА.
-
Иммунный ответ на Аг БГСА — продукция антистрептококковых АТ (антистрептолизина О, антистрептогиалуронидазы и др.), участвующих в формировании циркулирующих иммунных комплексов. Патологическое действие стрептококка проявляется его прямым повреждающим воздействием и токсическим влиянием продуцируемых им АТ, перекрестно реагирующих с его собственными тканями: Аг синовиальной мембраны суставов, ЦНС, сарколеммы кардиомиоцитов клапанов сердца, кожи (феномен молекулярной мимикрии).
Важной считают роль семейной предрасположенности, о чем свидетельствует семейная агрегация ревматической лихорадки, существенно превышающая распространенность заболевания в популяции. Генетическую предрасположенность к ОРЛ подтверждает выявление ряда генетических маркеров — группы крови А (0) и В (II), локусов системы HLA DR5-DR7, CW2-CW3, фенотипов кислой эритроцитарной фосфатазы, моноклональных АТ D 8/17, определяемых с высокой частотой у больных ОРЛ, что дает основание рассматривать их в качестве дополнительного диагностического критерия ОРЛ.
Патоморфология
Морфологические изменения отражают системную дезорганизацию соединительной ткани, особенно в сердечно-сосудистой системе, в которой выделяют 4 стадии:
-
мукоидное набухание;
-
фибриноидные изменения;
-
гранулематоз;
-
склероз, см.
.
Классификация
В настоящее время в клинической практике используют классификацию и номенклатуру ОРЛ (Ассоциация ревматологов России, 2003 г.; табл. 6.2).
|
Клинические варианты |
Клинические проявления |
Исход |
Стадия НК |
||
|
основные |
дополнительные |
КСВ |
NYHA |
||
|
ОРЛ. |
Кардит (вальвулит). |
Лихорадка. |
Выздоровление.
|
0 |
0 |
Примечание. НК — недостаточность кровообращения; КСВ — по классификации Стражеско– Василенко; NYHA — функциональный класс по New York Heart Association.
Клиническая картина
Острая ревматическая лихорадка
Характер дебюта ОРЛ связан с возрастом больных. В дошкольном возрасте через 2–3 нед после перенесенной ангины или фарингита у ребенка повышается температура до субфебрильных, реже фебрильных цифр и возникают мигрирующие боли, чаще в крупных суставах, нередко симметрично. Характерна высокая степень болезненности суставов. Одновременно появляются признаки кардита: сердцебиение, одышка, расширение границ сердца, приглушенность сердечных тонов, дующий систолический шум.
Для подростков и юношей характерно подострое, постепенное начало болезни: после перенесенной ангины сохранен субфебрилитет, общее недомогание, артрит или артралгии в крупных суставах, кардит с умеренными клиническими проявлениями.
Кардит является ведущим и наиболее тяжелым проявлением ОРЛ. Его диагностируют в 70–85% случаев заболевания. Обычно больные не предъявляют жалоб. Через 2–3 нед после перенесенной ангины не исчезает вялость, быстрая утомляемость, субфебрилитет. Редко (у 4–6%) выявляют субъективные симптомы со стороны сердца: кардиалгии, сердцебиение.
Основной критерий кардита — вальвулит преимущественно митрального клапана, характерный появлением на верхушке дующего, связанного с I тоном систолического шума. Иногда его сопровождает расширение границ сердца (преимущественно влево), приглушенность сердечных тонов различной степени выраженности и нарушения ритма (чаще — тахикардия), а также шум трения перикарда, свидетельствующий о вовлечении в процесс других оболочек сердца. Наличие признаков изолированного поражения мио- и перикарда (без вальвулита) ставит под сомнение диагноз ОРЛ и требует более углубленного обследования.
Ревматический полиартрит определяют в 60–100% случаев. Он характерен поражением крупных или средних суставов, носит мигрирующий характер, отличается доброкачественным течением, быстрой регрессией при назначении антиревматической терапии, не приводит к деструктивным изменениям суставов. Как правило, полиартрит сопровождают ревматический кардит или хорея.
Для ОРЛ у детей характерна малая хорея (ревматическая хорея, хорея Сиденгама, «пляска святого Витта»), встречаемая в 6–30%, преимущественно у девочек в возрасте от 6 до 15 лет. Основные ее симптомы обусловлены поражением подкорковых структур головного мозга и включают хореические гиперкинезы, мышечную гипотонию, нарушение координации движений, разнообразные психоэмоциональные и вегетативные расстройства.
Заболевание чаще начинается постепенно. Возникают эмоциональная лабильность, раздражительность, тревожность, неустойчивое настроение, импульсивность поступков, плаксивость, рассеянность, снижение памяти и концентрации внимания, ухудшение успеваемости. Позднее примыкают гиперкинезы и другие проявления малой хореи.
Гиперкинезы проявляются гримасничаньем, неловкими движениями, нечеткой речью, нарушением глотания, изменением почерка (рис. 6.1), походки. Они чаще носят двусторонний характер, возрастают при волнении, ослабевают в покое или прекращаются во время сна. Выраженность гиперкинезов варьирует от незначительных до массивных движений в различных группах мышц («хореическая буря»). Мышечная гипотония проявляется «симптомом дряблых плеч» с возможным развитием парезов мышц и полной обездвиженности больного («мягкая» хорея).

Рис. 6.1. Изменение почерка при малой хорее (до и после лечения)
Малую хорею могут сопровождать другие клинические проявления ОРЛ (кардит, артрит) либо она протекает изолированно, не сопровождаясь изменениями лабораторных показателей. Течение хореи часто имеет затяжной или рецидивирующий характер, продолжительность атаки может достигать 4–6 мес и больше.
Кольцевидную (анулярную) эритему (рис. 6.2) выявляют в 4–17% случаев, преимущественно при манифестном начале заболевания. Высыпания расположены преимущественно на коже груди, живота и проксимальных отделах конечностей.
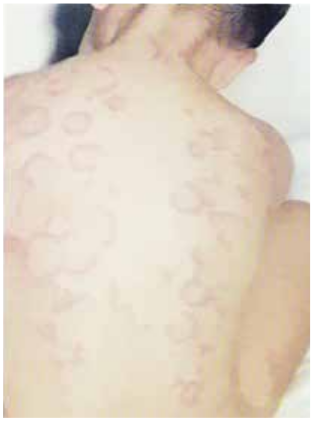
Рис. 6.2. Кольцевидная эритема при острой ревматической лихорадке
Подкожные ревматические узелки (рис. 6.3) в настоящее время у детей возникают чрезвычайно редко (в 1–3% случаев). Они представляют собой округлые, плотные, безболезненные и малоподвижные образования размером до 0,5–1 см, чаще всего расположенные в местах прикрепления сухожилий, на разгибательной поверхности суставов, вдоль остистых отростков позвонков и в затылочной области. По длительности ревматические узелки могут существовать не более 2–4 нед.
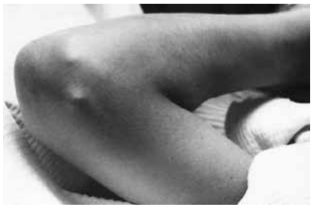
Рис. 6.3. Ревматические узелки
Поражение других органов. К числу тяжелых проявлений ОРЛ относят поражение серозных оболочек с развитием серозного перитонита с абдоминальным синдромом.
Хроническая ревматическая болезнь сердца
К проявлениям хронической ревматической болезни сердца (рис. 6.4) прежде всего относят клапанные пороки сердца, а также связанные с ними тромбоэмболический синдром, гемолитическую анемию и предсердную аритмию. Формирование клапанных пороков сердца отмечают в 20–25% случаев у детей и в 1/3 случаев у подростков. Преобладают изолированные пороки сердца, чаще недостаточность митрального клапана, реже — митральный стеноз, недостаточность или стеноз аортального клапана, а также комбинированные митрально-аортальные пороки. Приблизительно у 10% детей после ОРЛ развивается пролапс митрального клапана.
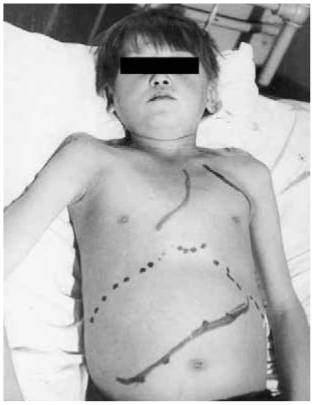
Рис. 6.4. Пациент с хронической ревматической болезнью сердца
Диагностика
В настоящее время применяют диагностические критерии ОРЛ, модифицированные Ассоциацией ревматологов России в 2003 г. (табл. 6.3).
| «Большие» критерии | «Малые» критерии | Данные, подтверждающие предшествовавшую А-стрептококковую инфекцию |
|---|---|---|
|
Кардит. |
Клинические |
Позитивная А-стрептококковая культура, выделенная из зева, или положительный тест быстрого определения А-стрептококкового Аг. |
* N — нормальное значение.
Наличие двух больших критериев или одного большого и двух малых, а также доказательства перенесенной БГСА-инфекции с большой степенью вероятности указывают на наличие у пациента ОРЛ. Данный подход обоснован при первой атаке ОРЛ. При повторном развитии ревматического процесса, рассматриваемого как новый случай заболевания, допустимо ограничить учет одним большим или только малыми критериями в сочетании с лабораторными данными, подтверждающими предшествовавшую стрептококковую инфекцию.
Лабораторные сдвиги характеризуют тенденцией к лейкоцитозу, повышением показателей СОЭ, серомукоида, диспротеинемией (увеличением фракции гамма-глобулинов), положительной реакцией на СРБ, нарастанием уровня Ig классов А, М и G. Особое место занимают серологические исследования, позволяющие установить наличие предшествовавшей БГ-СА-инфекции (титры противострептококковых АТ — антистрептолизина О и анти-ДНКазы В).
Нередко ОРЛ сопровождается повышением уровня АТ к кардиолипину класса IgG, уровня неоптерина (отражает активацию моноцитов/макрофагов и Т-лимфоцитов в связи с повышением уровня рИЛ-2Р). Для ОРЛ характерна частая встречаемость Аг гистосовместимости Dr5-Dr7, Cw2-Cw3, а также аллоантигена В-лимфоцитов (в 90% случаев), определяемого с помощью моноклональных АТ D8/17.
Рентгенологически определяют кардиомегалию, изменение конфигурации сердечной тени (митральную или аортальную в зависимости от локализации вальвулита), а также, при наличии сердечной декомпенсации, застойные явления в легких.
На ЭКГ выявляют нарушения сердечного ритма, чаще в виде тахикардии, АВ-блокады I–II степени, миграцию водителя ритма, экстрасистолии и нарушение процессов реполяризации желудочков. В тяжелых случаях можно наблюдать фибрилляцию предсердий и другие формы аритмий.
ЭхоКГ позволяет выявить признаки вальвулита (рыхлость и утолщение створок пораженных клапанов, ограничение их подвижности, клапанную регургитацию) и оценить морфо-функциональное состояние сердца в целом, включая характеристику гемодинамических показателей.
Дифференциальная диагностика
Нередко у детей впервые регистрируют сердечные шумы, что не исключает их ревматического происхождения. При этом необходимо учитывать наличие ВПС, не установленного ранее, а также малых сердечных аномалий. Последнюю группу выявляют в виде пролапса митрального клапана, аномальных трабекул в полости левого желудочка, изменений аорты и др., которые могут быть расценены как проявление клапанного повреждения при ОРЛ. Выявление внешних проявлений соединительнотканной дисплазии, тщательный анализ результатов клинико-инструментального обследования, особенно данных ЭхоКГ, отсутствие анамнестических сведения ревматического характера позволяют поставить под сомнение диагноз ОРЛ.
При отсутствии значимых признаков поражения клапанного аппарата сердца необходимо проведение дифференциальной диагностики ОРЛ и неревматических кардитов. Для последних характерно развитие кардиальных нарушений в тесной взаимосвязи с вирусной инфекцией, отсутствие клинических и лабораторных проявлений, определяемых при ОРЛ.
Артралгии или артрит, сопровождаемые экссудативными изменениями в суставах, могут сопутствовать другим болезням ревматического профиля [системной красной волчанке (СКВ), ювенильному идиопатическому артриту (ЮИА)] или быть следствием различных перенесенных инфекционных заболеваний, включая стрептококковую инфекцию (постстрептококковый реактивный артрит). Для большинства из них разработаны диагностические критерии.
Клинические проявления малой хореи могут напоминать неврологические расстройства, наблюдаемые при СКВ, узелковом полиартериите и других васкулитах, при антифосфолипидном синдроме (АФС), онкогематологической патологии, синдромах Туретта, PANDAS[4] и ряде других состояний.
Синдром Туретта возникает в 5–6-летнем возрасте, чаще (в отличие от малой хореи) среди мальчиков, характерен внезапно возникающими насильственными подергиваниями мышц лица (мигание, высовывание языка), шеи, плечевого пояса, появлением резких, размашистых движений, непроизвольным произнесением слов или звуков (вокальные тики), сквернословия (копролалия).
Синдром PANDAS (Pediatric Autoimmune Neuropsychiatric Disorders Associated with Streptococcal Infections) напоминает ревматическую хорею, развивается среди детей препубертатного возраста в связи с предшествовавшей БГСА-инфекцией, характерен вариабельностью клинических проявлений (обессивно-конвульсивные расстройства, двигательная реактивность, хореиформные гиперкинезы), высокой частотой выявления аллоантигенов лимфоцитов D8/17, а также регрессированием психоневрологической симптоматики под влиянием противострептококковой антибактериальной терапии.
Лечение
Тактика ведения больных с ОРЛ основана на принципах комплексного 3-этапного лечения, включающего стационарное лечение (1-й этап), долечивание в местном ревматологическом санатории (2-й этап) и диспансерное наблюдение в поликлинике (3-й этап) (см. ).
1-й этап
При легком течении назначают полупостельный (на 7–10 дней), а при более тяжелом — строгий постельный режим (на 15–20 дней). Расширение двигательной активности допускают при улучшении клинических и лабораторных показателей.
Этиотропное лечение включает обязательное применение препаратов пенициллинового ряда [феноксиметилпенициллин (Оспен♠), амоксициллин (Флемоксин солютаб♠) и др.]. При их непереносимости назначают антибиотики из групп цефалоспоринов или макролидов. Антибактериальную терапию проводят не менее 14 дней, в последующем переходят на введение пролонгированных форм пенициллина.
Антиревматическая терапия включает НПВП [диклофенак, индометацин, нимесулид (Нимулид♠) применяется в течение не менее 1–1,5 мес до ликвидации признаков активности процесса] и (по показаниям) глюкокортикоиды в среднем 1–1,5 мес с последующей отменой (преднизолон в течение 10–14 дней до получения клинического эффекта; затем суточную дозу снижают по 2,5 мг каждые 5–7 дней под контролем клинико-лабораторных показателей). Продолжительность применения хинолиновых производных составляет от нескольких месяцев до 1–2 лет и более в зависимости от течения заболевания.
Медикаментозная терапия ОРЛ у детей представлена в табл. 6.4.
| Вид терапии | Наименование и доза препарата | Показания к применению |
|---|---|---|
|
Антибактериальная |
Препараты пенициллинового ряда: феноксиметилпенициллин — 100 мг/кг в сут, амоксициллин — 0,1 г/кг в сут (Флемоксин солютаб♠ — 30 мг/кг в сут) |
Наличие тонзиллофарингита, обусловленного БГСА |
|
Антиревматическая |
НПВП: диклофенак — 2–3 мг/кг в сут, индометацин — 2–3 мг/кг в сут, нимесулид (Нимулид♠, суспензия) — 1,5 мг/кг в сут |
Низкая степень активности. Изолированный суставной синдром. |
|
Глюкокортикоиды: преднизолон — 0,7–0,8 мг/кг в сут (не более 1 мг/кг в сут) |
Высокая или умеренная степень активности. |
|
|
Хинолиновые производные (хлорохин, гидроксихлорохин) — 0,06–0,25 г/сут |
Затяжное течение |
|
|
Симптоматическая |
Диуретики: Сердечные гликозиды: |
Острая или хроническая сердечная недостаточность |
|
Другие препараты: аскорбиновая кислота и витамины группы В, антигистаминные средства, триметазидин (Предуктал♠), карнитин, поливитамины + прочие препараты (Вирум бьюти коэнзим Q10♠), антиаритмические, седативные средства и др. |
В зависимости от особенностей клинической картины и фазы заболевания |
Немаловажное значение в терапии ОРЛ имеют симптоматические методы лечения. При сердечной недостаточности используют диуретики, вазодилататоры, ингибиторы ангиотензин-превращающего фермента, β-адреноблокаторы и сердечные гликозиды, применяемые в зависимости от наличия декомпенсированной или стабильной формы хронической сердечной недостаточности.
В терапии сердечной недостаточности важную роль отводят коррекции энергетических процессов в миокарде с использованием триметазидиа (Предуктала♠), левокарнитина, цитохрома С, коэнзима Q10♠, поливитаминов. При необходимости назначают антиаритмические препараты.
Наличие симптомов малой хореи требует применения препаратов, снижающих активность дофаминергических систем головного мозга — галоперидола, производных фенотиазина и др.
По показаниям проводят санацию хронических очагов инфекции. Тонзилэктомия может быть осуществлена через 2–2,5 мес. от начала заболевания при отсутствии признаков активности процесса.
2-й этап
2-й этап предусматривает достижение полной ремиссии и восстановление функциональной способности сердечно-сосудистой системы. Продолжают начатую в стационаре терапию, санируют очаги хронической инфекции, осуществляют индивидуально подобранный комплекс лечебно-оздоровительных мероприятий (ЛФК, закаливающие процедуры).
3-й этап
3-й этап предусматривает диспансерное наблюдение за пациентами, перенесшими ревмокардит, направлен на профилактику рецидивов и прогрессирования заболевания. В течение первого года после поступления ребенка на учет наблюдение проводят ежемесячно, в последующем — ежеквартально.
Дальнейший контроль проводят 2 раза в год. Амбулаторное обследование включает необходимые лабораторные и инструментальные методы диагностики, консультации ЛОР-врача и стоматолога. Кроме того, назначают необходимые оздоровительные мероприятия, ЛФК. В период диспансерного наблюдения продолжают ранее начатую вторичную профилактику.
Профилактика
Выделяют первичную и вторичную профилактику ОРЛ. Основу первичной профилактики составляет комплекс мероприятий, направленных на укрепление здоровья детей и подростков, раннюю диагностику и адекватную терапию стрептококковой инфекции, вызванной БГСА (хронический тонзиллит, фарингит). Особое внимание следует уделять детям, проживающим в неблагоприятных социально-бытовых условиях, в семьях которых отмечены случаи ОРЛ или другие заболевания ревматического профиля, а также часто болеющим инфекцией верхних дыхательных путей и имеющим хронический тонзиллит.
Лечение острой и хронической БГСА-инфекции осуществляют с использованием амоксициллина или, при необходимости, других препаратов, упоминавшихся ранее при характеристике методов этиотропного лечения ОРЛ.
Вторичная профилактика ОРЛ основывается на введении следующих препаратов.
-
Бензатина бензилпенициллин + бензилпенициллин прокаина (Бициллин-5♠): школьникам и подросткам — 1 500 000 ЕД 1 раз в 3–4 нед, детям дошкольного возраста — 750 000 ЕД 1 раз в 2 нед.
-
Бензатина бензилпенициллин (Бициллин-1♠): детям дошкольного возраста — 600 000 ЕД 1 раз в 2 нед, детям школьного возраста — 1 200 000 ЕД 1 раз в мес.
-
Для вторичной профилактики ОРЛ рекомендуют введение бензатина бензилпенициллин (Экстенциллин♠): детям по 600 000–1 200 000 ЕД в зависимости от массы тела, подросткам и взрослым — 2 400 000 ЕД (1 раз в
3 нед).
Рациональной считают круглогодичную профилактику, начинающуюся уже в стационаре. Ее продолжительность определяют индивидуально. У детей, перенесших ОРЛ без вовлечения сердца (артрит, малая хорея), ее длительность составляет не менее 5 лет после последней атаки или до достижения 18-летнего возраста, а при наличии кардита без формирования порока сердца — не менее 10 лет или до возраста 25 лет (по принципу «что дольше»). Пациентам с пороком сердца, в том числе после хирургической его коррекции, вторичную профилактику проводят пожизненно.
Прогноз
Определяющее значение имеет характер сердечных нарушений (локализация, степень распространенности и выраженности патологического процесса, наличие клапанного повреждения). Диффузный миокардит, сопровождаемый сердечной декомпенсацией, оказывает неблагоприятное влияние на прогноз ОРЛ.
При своевременно начатом лечении прогноз (при отсутствии сформировавшегося порока сердца) относительно благоприятный. Хроническая ревматическая болезнь сердца, особенно при наличии пороков сердца, способных прогрессировать и приводить к стойкой сердечной декомпенсации, имеет неблагоприятное прогностическое значение.
Тестовые задания
-
Для кардита при ОРЛ наиболее характерны:
-
вальвулит митрального клапана;
-
частое вовлечение в процесс аортального клапана;
-
наличие кардита с другими проявлениями ОРЛ;
-
все вышеперечисленное.
-
-
Полиартрит при ОРЛ характеризуют:
-
симметричным олигоартритом (реже моноартритом);
-
«летучестью» суставного синдрома;
-
быстрой регрессией при назначении антиревматической терапии;
-
всем перечисленным выше.
-
-
Что из нижеперечисленного нехарактерно для малой хореи?
-
может протекать без других проявлений ОРЛ (кардит, полиартрит);
-
нередко имеет затяжной или рецидивирующий характер течения;
-
с одинаковой частотой выявляется во всех возрастных группах;
-
значительно чаще регистрируется у девочек.
-
-
У 12-летнего ребенка диагностирована ОРЛ (активность III степени, эндомиокардит, полиартрит). На фоне проводимой терапии через 1,5 мес отмечена положительная динамика, однако полной нормализации клинических и лабораторных показателей не произошло. В лечении данного больного необходимо использовать:
-
антибиотики;
-
НПВП;
-
глюкокортикоиды;
-
все вышеперечисленное.
-
-
Мальчик в возрасте 10 лет перенес ОРЛ с кардитом, без формирования порока сердца. В данном случае длительность проведения вторичной профилактики должна быть:
-
1 год;
-
3 года;
-
5–7 лет;
-
10 лет и более.
-
Ответы: 1 — a; 2 — d; 3 — c; 4 — d; 5 — d.
Литература
-
Кузьмина Н.Н., Щербакова М.Ю. Ревматизм (острая ревматическая лихорадка). Кардиология и ревматология детского возраста // Практическое руководство по детским болезням. Т. III / под ред. Г.А. Самсыгиной, М.Ю. Щербаковой; под общ. ред. В.Ф. Коколиной, А.Г. Румянцева. М. : Медпрактика-М, 2004. С. 479–493.
-
Острая ревматическая лихорадка : национальное руководство по ревматологии / под ред. Е.Л. Насонова, В.А. Насоновой. М. : ГЭОТАР-Медиа, 2008. С. 400–418.
-
Руководство по детской ревматологии / под ред. Н.А. Геппе, Н.С. Подчерняевой, Г.А. Лыскиной. М. : ГЭОТАР-Медиа, 2011.
-
Rheumatic fever and rheumatic heart disease: report of a WHO Expert Consultation. Geneva, 29 October — 1 November, 2001 // WHO Technical Report Series. 2004. Vol. 923. P. 122.
-
van Toorn R., Weyers H.H., Schoeman J.F. Distinguishing PANDAS from Sydenham’s chorea: case report and review of the literature // Eur. J. Paediatr. Neurol. 2004. Vol. 8, N 4. P. 211–216.
Виталий Омельченко
«Наука из первых рук» № 2/3 (78), 2018
Что такое медицина — искусство или наука? Начав с интуитивных манипуляций и постепенно накапливая опыт, «лечебное искусство» все активнее интегрировало чисто научные методы и подходы. В истории медицины как науки можно выделить переломные моменты, связанные с открытиями микроорганизмов, механизмов иммунитета и другими фундаментальными достижениями. В результате появился целый ряд новых медицинских дисциплин, в том числе ревматология, о которой мало знают не только пациенты, но и врачи других специальностей.
Об авторе
Виталий Олегович Омельченко — врач-ревматолог, врач-терапевт ревматологического отделения, младший научный сотрудник лаборатории патологии соединительной ткани Научно-исследовательского института клинической и экспериментальной лимфологии — филиала Института цитологии и генетики СО РАН (Новосибирск), аспирант кафедры терапии, гематологии и трансфузиологии ФПК и ППВ Новосибирского государственного медицинского университета. Автор и соавтор 18 научных работ.
Благодаря опорному «каркасу», сформированному соединительной тканью, мы радикально отличаемся от «жидких» амеб. К соединительной ткани относят, к примеру, кровь и лимфу, кости и хрящи; она входит в состав жировой клетчатки и слизистой. Эта ткань связывает все воедино, составляя половину нашего тела и выполняя не только опорную, но и защитную и трофическую функции.
Заболеваниями соединительной ткани занимается ревматология — одна из самых молодых специальностей, получившая самостоятельность лишь в середине XX в., хотя еще во II в. знаменитый античный врач Гален ввел термин «ревматизм» для общего обозначения заболеваний опорно-двигательного аппарата. Но только с XVII в. стали появляться описания отдельных болезней, а быстрое развитие ревматологии в последние десятилетия было вызвано как открытиями механизмов иммунитета, так и улучшением диагностических возможностей.
В наши дни, по данным ВОЗ, около 100 млн европейцев страдают различными ревматологическими заболеваниями. О реальной ситуации в нашей стране судить трудно, так как учет заболеваемости ведется только по наиболее серьезному заболеванию пациента (например, при одновременном наличии сердечной патологии будет учитываться только она одна). Между тем по затратам на лечение ревматология немногим уступает самой «дорогостоящей» области медицины — онкологии, что связано с необходимостью постоянного приема весьма недешевых препаратов, отмена которых может спровоцировать всплеск болезни.
Поскольку соединительная ткань есть везде, то и ревматологам приходится иметь дело с разнообразным проявлением заболеваний, поражающих не только суставы, но и сердце, легкие, почки, нервную систему и т. д. Поэтому практически всегда ревматологи должны работать в тесной связке с другими специалистами. К сожалению, немногие из врачей других специальностей, не говоря уже о пациентах, хорошо знакомы с ревматологией. А так как самих ревматологов крайне мало, то необоснованные направления на обследования не позволяют вовремя попасть на консультации людям, действительно нуждающимся в специальном лечении.
В основе ревматологических заболеваний чаще всего лежит аутоиммунный процесс, при котором иммунная система организма начинает воспринимать собственные ткани как чужеродные и повреждать их в результате воспаления. Первопричина же в большинстве случаев неизвестна: считается, что такие патологические реакции иммунной системы обусловлены взаимодействием факторов наследственной природы и окружающей среды.
Что лечим?
Число ревматологических заболеваний достигает сотни, но лишь некоторые из них встречаются достаточно часто. Сложность их диагностики в том, что одна и та же болезнь может иметь множество различных проявлений, а разные болезни — схожие симптомы. Каждый ревматологический больной — это загадка, и правильная расстановка акцентов напрямую связана с опытом и квалификацией врача.
Самый распространенный симптом (не болезнь!), с которым пациенты попадают на прием, — артрит, общее название для боли и припухлости сустава. Есть более сотни различных видов артрита и, соответственно, ассоциированных с ними патологических состояний. При этом важно различать поражения непосредственно сустава и околосуставных тканей, так как боль, припухлость и скованность часто бывают результатом травм, лечением которых ревматология напрямую не занимается.
«Наша» болезнь — остеоартрит, в его основе лежит истончение хряща, который в норме выполняет амортизационную функцию: при наличии синовиальной (внутрисуставной) жидкости коэффициент трения двух хрящевых поверхностей в 15 раз ниже, чем между двумя кубиками льда.
Основные факторы развития остеоартрита — пожилой возраст, травма и выполнение однотипных, часто повторяющихся движений. Повреждение хряща приводит к «царапанию» надкостницы остеофитами (патологическими костными наростами) и растяжению капсулы сустава, что вызывает ноющую боль, усиливающуюся при нагрузке. Интересно, что степень болезненности не всегда соответствует степени поражения сустава: у 90% людей старше 40 лет есть рентгенологические признаки остеоартрита, но лишь треть из них жалуются на боли (Харрисон, 2005). В большинстве случаев постоянного лечения у ревматолога даже и не требуется: достаточно наблюдаться у терапевта и соблюдать рекомендации. Ранее считалось, что остеоартрит является полностью дегенеративным заболеванием, но в последние годы получены доказательства роли воспаления в развитии этой патологии.
Однако существуют и истинно воспалительные артриты. Их типичным представителем является ревматоидный артрит — аутоиммунное заболевание соединительной ткани, поражающее преимущественно мелкие суставы (иногда в процесс могут вовлекаться легкие, система кроветворения, сосуды). Эта болезнь имеет черты онкологического процесса, поскольку в его основе лежит неконтролируемое разрастание ткани синовиальной оболочки, выстилающей суставы, что приводит к необратимому повреждению сустава.
Ревматоидный артрит развивается при потере иммунологической толерантности к собственным тканям организма. Провоцирующий фактор неизвестен, а появление аутоантител и постепенное повышение С-реактивного белка, характерного маркера воспалительного процесса, отмечается еще за несколько лет до первого обращения к врачу. Начинается болезнь в молодом возрасте (30–35 лет), причем женщины страдают в 3 раза чаще мужчин. Генетические маркеры, свидетельствующие о предрасположенности к развитию этого заболевания, известны, но однозначно они с ним не ассоциированы. Механизм развития заболевания пока неясен и активно изучается во всем мире.
После появления первых симптомов примерно в течение полугода существует возможность если не полностью обратить процесс вспять, то хотя бы «пригасить» его и не допустить разрушения тканей. Успех зависит от раннего и достаточно серьезного лечения. Для своевременной диагностики очень важно обратить особое внимание на следующие признаки, которые говорят о срочной необходимости посетить ревматолога: утренняя скованность более получаса, припухлость или болезненность трех и более суставов, слабость в кистях рук и боль при тесте поперечного сжатия кисти.
Утром болит спина?
Еще один важный симптом ревматологического заболевания — воспалительная боль в спине. И это не та боль, которая возникает после тяжелой физической нагрузки и проходит после отдыха: в этом случае спина болит утром, когда человек только проснулся.
Согласно статистике, молодой пациент с подобными жалобами может до 10 лет мигрировать между различными специалистами — неврологами, ортопедами, терапевтами — с такими диагнозами, как «остеохондроз», «межпозвонковая грыжа» и т. д., пока, наконец, не попадет к ревматологу (Дубинина, Эрдес, 2010). И за это время у него сформируются необратимые изменения, которых можно было бы избежать при своевременной диагностике.
Воспалительная боль в спине сопровождает целую группу заболеваний, именуемую спондилоартропатией, при которых поражаются суставы позвоночника.
Типичным представителем данной группы является анкилозирующий спондилит, или болезнь Бехтерева — хроническое воспалительное заболевание позвоночника и крестцово-подвздошных сочленений, протекающее также с поражением периферических суставов и участков прикрепления связочно-сухожильного компонента сустава к кости, поражением глаз (увеит) и луковицы аорты (аортит) (Ревматология: национальное руководство, 2008).
Ранее считалось, что болезнь Бехтерева поражает только мужчин, но не так давно его активно начали выявлять у женщин. Кроме того, у женщин клиническая картина имеет свои особенности: чаще поражается шейный отдел позвоночника, для начала болезни характерен периферический артрит, более доброкачественное течение заболевания в целом. Общепризнанным предрасполагающим фактором служит носительство одного из генов главного комплекса гистосовместимости HLA B 27. Но не надо сразу паниковать: хотя 90% больных имеют этот ген, среди его носителей болезнь развивается лишь в 1–2% случаев. Однако, помимо HLA B 27, выявлено еще более шести десятков потенциально «рискованных» генных локусов (Ranganathan, 2017).
Покой таким больным противопоказан: они должны заниматься зарядкой не менее получаса 4 раза в день, чтобы сохранить подвижность позвоночника. При отсутствии регулярной правильной физической нагрузки быстро наступают необратимые изменения, что приводит к инвалидности.
Характерным признаком псориатического артрита (поражения суставов и позвоночника у больных псориазом) служат дактилиты — воспалительные процессы в пальцах кисти или стопы. При этом у 70% больных псориазом поражение кожи возникает раньше поражения суставов (Коротаева, Корсакова, 2018).
Считается, что развитие этого заболевания связано с активацией клеточного иммунитета и смещением баланса в сторону воспаления. В отличие от болезни Бехтерева, в этом случае поражаются преимущественно периферические суставы, а не позвоночник. Часто страдают дистальные межфаланговые суставы, которые при ревматоидном артрите практически не поражаются из-за отсутствия в них синовиальной оболочки.
Еще одно заболевание из группы спондилоартритов — реактивный артрит — возникает в результате строго определенных кишечных или половых инфекций. Большинство случаев связано с поражением хламидиями. Но, поскольку выделение самих микроорганизмов из сустава не увенчалось успехом, была выдвинута теория иммуноопосредованного воспаления в результате действия комплексов антиген-антитело. Начало заболевания приходится на возраст 20–40 лет, причем и в этом случае мужчины заболевают гораздо чаще женщин.
Спондилоартрит, ассоциированный с воспалительными заболеваниями кишечника, имеет много общих симптомов с другими спондилоартритами. Что является первичным поражением — воспалительный процесс в кишечнике или поражение опорно-двигательного аппарата — до сих пор остается предметом дискуссий.
В случае, когда имеются все признаки спондилоартропатии, но картина не укладывается ни в один из критериев определенного заболевания, устанавливается диагноз недифференцированного спондилоартрита. Это, по крайней мере, позволяет начать лечение на ранней стадии патологического процесса.
Широким фронтом
Системные заболевания соединительной ткани названы так из-за отсутствия «излюбленных» мест, которые поражает болезнь, и неспецифичности поражения соединительной ткани и ее производных. Одно из самых известных и распространенных заболеваний этой группы — системная красная волчанка, получившая свое название за характерное поражение кожи лица, похожее на укус волка. Это крайне многоликое заболевание, поистине ревматологическое, поскольку поражает все органы и системы организма за счет выработки органонеспецифических аутоантител и иммунных комплексов. Заболевают чаще всего молодые женщины, включая подростков. Обнаружены и генетические детерминанты (гены HLA B 8, DR 2, DR 3 и др.), позволяющие говорить о предрасположенности к болезни.
Системная красная волчанка встречается не так уж и редко (1 случай на 20 тыс. человек), поэтому важно знать симптомы, позволяющие заподозрить эту патологию: реакция на солнце (фотосенсибилизация) в виде сыпи, язвочки в полости рта, выпадение волос, синдром Рейно (приступообразный спазм кровеносных сосудов конечностей, когда под воздействием холода или стресса пальцы последовательно белеют, синеют и краснеют). Но бывает и так, что единственным проявлением заболевания может быть постоянная слабость и утомляемость. При отсутствии лечения прогноз зависит от активности процесса.
Другим грозным заболеванием в этой группе является системная склеродермия — полиорганное заболевание неизвестной этиологии, характеризующееся фиброзом кожи, сосудов и внутренних органов, в том числе желудочно-кишечного тракта, легких, сердца и почек (Харрисон, 2005). Увы, достаточно эффективные методы лечения этого заболевания пока не существуют: мы можем лишь отчасти замедлить начавшийся процесс, частично предотвращая и исправляя осложнения. К первым симптомам заболевания относятся синдром Рейно, плотный отек кожи, артриты и артралгии. По мере прогрессирования болезни кожа уплотняется и атрофируется, сосудистые и трофические нарушения усугубляются, поражаются внутренние органы. Диагностика заболевания основана на характерных клинических проявлениях, а также выявлении в крови иммунологических маркеров.
Но не все заболевания соединительной ткани ассоциированы с аутоиммунным процессом: в возникновении некоторых из них «виновато» нарушение обмена веществ. Наиболее известным и распространенным таким заболеванием является подагра. Клинические признаки самого яркого ее проявления — подагрического артрита — описал в свое время еще знаменитый Гиппократ. В основе заболевания лежит нарушение обмена веществ и повышение в крови уровня мочевой кислоты. Это приводит к накоплению мочевой кислоты в тканях, в первую очередь в суставах (чаще всего большого пальца стопы), где она откладывается в виде кристаллов соли натрия. К этому месту подтягиваются макрофаги-«мусорщики», и начинается воспалительный процесс.
Подагру недаром называют «болезнью аристократов»: основной причиной развития заболевания служат неправильная диета, в первую очередь избыток мясной пищи, а провоцируют его злоупотребление алкоголем, малоподвижный образ жизни или, напротив, чрезмерные физические нагрузки. Без соблюдения диеты эффективное лечение подагры невозможно! Хотя существуют препараты, снижающие уровень мочевой кислоты, но если на фоне их приема нарушить диету, симптомы все равно разовьются.
Причины накопления солей мочевой кислоты, которая в норме должна выделяться через почки, остаются до конца непонятными. Известно только, что у большинства подагриков имеется наследственная предрасположенность к этой болезни. Интересный факт: еще в 1955 г. англичанин Э. Орван указал на структурное молекулярное сходство мочевой кислоты с кофеином и теобромином, которые, как известно, служат стимуляторами умственной активности. Исследователь даже высказал предположение, что именно отсутствие у приматов фермента уриказы, расщепляющего мочевую кислоту у других млекопитающих, стало одной из предпосылок появления среди них человеческого разума. К этому можно лишь добавить, что число подагриков среди признанных талантов и гениев намного больше, чем среди обычных людей.
Чем лечим?
Поскольку большинство ревматологических заболеваний неразрывно связано с воспалением, открытие в 1948 г. глюкокортикоидов, позволяющих эффективно подавлять этот процесс, кардинально изменило ситуацию с лечением. Однако с течением времени стало ясно, что нужно искать другие препараты, поскольку применение гормонов чревато большим числом неблагоприятных побочных эффектов.
Помимо глюкокортикоидов, в лечении используются нестероидные противовоспалительные средства и синтетические базисные противовоспалительные препараты, к которым относят сульфасалазин, метотрексат, лефлуномид, циклофосфамид, азатиоприн, плаквенил. Большинство последних средств было создано для терапии онкологических заболеваний или для нужд трансплантологии. Проще говоря, сейчас ревматологи используют очень сильные фармакологические препараты, направленные на подавление иммунной системы. Можно сказать, мы лечим почти так же агрессивно, как онкологи. Но последние убивают ту ткань, с которой не может справиться иммунная система организма, мы же, напротив, подавляем саму слишком активную иммунную систему.
Самым популярным препаратом этой группы является метотрексат, который используется здесь в гораздо меньших дозировках, чем в онкологической практике. Он очень эффективно уменьшает воспаление, препятствуя возникновению осложнений, и при этом достаточно безопасен при условии контроля за основными показателями крови.
Важным прорывом в лечении ревматологических заболеваний стало открытие моноклональных антител, способных подавлять основные пути развития воспаления, и создание соответствующих генно-инженерных биологических препаратов. Самые популярные такие препараты воздействуют на ряд мишеней: В-лимфоциты, провоспалительные цитокины, системы внутриклеточной передачи сигнала.
Конечно, и эти средства не лишены недостатков: они, в принципе, могут вызывать инфекционные осложнения, способствовать развитию анафилактических реакций и т. д., поэтому также нуждаются в тщательном контроле при применении. В НИИ клинической и экспериментальной лимфологии существует антицитокиновый центр с хорошими реанимационными возможностями, где подобные препараты используют для терапии пациентов при постоянном мониторинге показателей жизнедеятельности.
К сожалению, даже самое современное медикаментозное лечение не всегда приводит к положительному результату, и в этом случае на помощь приходит хирургия. В нашей клинике, в частности, проводятся операции по замене пораженных суставов — тазобедренных и коленных, а также другие хирургические вмешательства. Благодаря тесному сотрудничеству с хирургической службой у наших специалистов есть возможность непосредственно изучать биопсийный материал из пораженных суставов, что расширяет исследовательские возможности.
Этот небольшой обзор не претендует на полноту, так как существует еще много заболеваний ревматологического профиля, здесь не упомянутых, но вполне актуальных. Его цель — дать общие представления о наиболее важных моментах ревматологической практики и акцентировать внимание на необходимости наблюдения за любыми, даже самыми незначительными на первый взгляд проявлениями. Ведь диагностические протоколы, основанные на современных методах обследования, могут выявить такую болезнь уже на ранних стадиях. Но пока основной проблемой является недостаточная информированность самих больных и даже специалистов другого профиля.
Несмотря на молодой возраст, ревматология стремительно развивается, постоянно расширяя свои возможности как в диагностике, так и в лечении. И ключевую роль в этом играет тесное взаимодействие ученых и медиков, другими словами, научных институтов и клинических отделений. Именно в таком сотрудничестве кроются большие перспективы для поиска первопричин и механизмов развития заболеваний, а также новых методов диагностики и терапии болезней, которые приобретают все большее значение в современном обществе.
Автор благодарит сотрудников ревматологогического отделения клиники НИИКЭЛ (Новосибирск) за помощь в подготовке иллюстративного материала.
Статья подготовлена на основе публичной лекции, прочитанной автором в июне 2018 г. в одном из баров новосибирского Академгородка во время «Ночи научных историй», которую организовала команда фестиваля EUREKA! FEST.
Литература
1. Внутренние болезни по Тинсли Р. Харрисону: В 7 т.; пер. с англ. / Под ред. Э. Фаучи, Ю. Браунвальда и др. Практика, Мак-Гроу-Хилл (совместное издание), 2005. 491 с.
2. Дубинина Т. В., Эрдес Ш. Ф. Причины поздней диагностики анкилозирующего спондилита в клинической практике // Научно-практическая ревматология. 2010. Т. 48. № 2. С. 43–48.
3. Коротаева Т. В., Корсакова Ю. Л. Псориатический артрит: классификация, клиническая картина, диагностика, лечение // Научно-практическая ревматология. 2018. Т. 56. № 1. С. 60–69.
4. Ревматология: национальное руководство / Под ред. Е. Насонова, В. Насоновой. М.: ГЭОТАР-Медиа, 2008. 720 с.
5. Ranganathan V., Gracey E., Brown M. A. et al. Pathogenesis of ankylosing spondylitis — recent advances and future directions // Nat. Rev. Rheumatol. 2017. V. 13, N. 6. P. 359–367.
Ревматические заболевания у детей в настоящее время широко распространены, и частота их возникновения неуклонно растет. Значительную часть этой патологии занимают заболевания суставов. Симптомы поражения суставов могут возникать постепенно или развиваться остро, а в случае хронизации процесса нередко приводят к инвалидизации ребенка, нарушая его рост, развитие и социальную адаптацию. В данной статье описаны особенности суставного синдрома при наиболее распространенных заболеваниях суставов у детей.
Ювенильный идиопатический (ревматоидный) артрит (ЮРА) определяется как артрит неустановленной причины, присутствующий в течение 6 недель, возникший у ребенка, не достигшего 16-летнего возраста, при исключении другой патологии суставов (Классификация и номенклатура ювенильных идиопатических артритов, Дурбан, 1997).
Классификация и номенклатура ЮРА включает выделение семи вариантов течения заболевания (по классификации Международной лиги ревматологических ассоциаций (League of Associations for Rheumatology, ILAR)):
1) системный артрит;
2) полиартрит: негативный по ревматоидному фактору (РФ);
3) полиартрит: позитивный по РФ;
4) олигоартрит: а) персистирующий, б) распространяющийся;
5) энтезитный артрит;
6) псориатический артрит;
7) другие артриты, которые а) не соответствуют ни одной из категорий или б) отвечают критериям более чем одной категории.
Системная форма с полиартритом (соответствует синдрому Стилла)
Этот системный вариант ЮРА был впервые описан британским педиатром Д. Ф. Стиллом в 1897 г. В настоящее время, по данным литературы и нашим наблюдениям, синдром Стилла встречается достаточно редко, всего в 12–16% от всех случаев ЮРА у детей, преимущественно раннего возраста [1–4]. Для него характерно острое, манифестное, начало; на самых ранних этапах болезни в процесс вовлекаются как крупные, так и мелкие суставы, в том числе мелкие суставы кистей и стоп. Для синдрома Стилла типично вовлечение в процесс шейного отдела позвоночника и височно-нижнечелюстных суставов. Суставы припухшие, резко болезненные, в них могут быстро развиться болевые контрактуры. Боль и контрактуры приводят к потере функции и вынужденному положению пораженного сустава под определенным углом, в результате чего дети теряют подвижность. Таким образом, кардинально от других вариантов ЮРА, этот вариант отличает генерализованный суставной синдром в дебюте. Для этого варианта ЮРА также характерны внесуставные проявления. Самые частые из них — лихорадочный синдром и сыпь. Лихорадка чаще фебрильная, иногда достигающая 39–40 °С, продолжающаяся, как правило, не более 3–4 недель. Сыпь при синдроме Стилла чаще мелкоточечная, напоминающая скарлатинозную, иногда — кореподобную, нестойкая, более выраженная на высоте лихорадки. Процент инвалидизации при синдроме Стилла достигает 25–30% [2].
Системная форма ЮРА с ограниченным суставным синдромом или олигоартритом, соответствующая аллергосептическому варианту
Впервые симптомокомплекс, включающий в себя лихорадку, артралгии, аллергическую сыпь, лимфаденопатию, гепатоспленомегалию и сопровождающийся высоким нейтрофильным лейкоцитозом, был описан Висслером в 1943 г. В последующем, наблюдая около 100 подобных случаев, Висслер и Фанкони пришли к выводу, что это заболевание имеет аутоиммунную природу и нередко трансформируется в ревматоидный артрит. Он существенно отличается от синдрома Стилла, прежде всего отсроченностью суставных проявлений, что значительно затрудняет раннюю диагностику. Мы наблюдали детей, у которых стойкие симметричные изменения в суставах сформировались только через 2–3 года от начала заболевания. Локализация суставных поражений также своеобразна. Как правило, в процесс вовлекаются крупные суставы — коленные, тазобедренные, голеностопные и очень редко — суставы кистей и стоп. В них довольно быстро развиваются деструктивные изменения: разволокнение хряща, костные эрозии, причем этот процесс быстро прогрессирует, приводя к значительному разрушению, например, головки бедренной кости. Для этого варианта заболевания свойственен и особый характер лихорадки: обычно она появляется в ранние утренние часы, начиная с 5–6 часов, после сильного озноба. Продолжительность лихорадки — 3–4 часа, затем наступает гектическое падение, сопровождающееся проливными потами. Начало лихорадки часто совпадает с появлением кожных высыпаний. Сыпь при аллергосептическом синдроме носит чрезвычайно упорный характер и, также как лихорадка, может длиться месяцами. Локализуется она на туловище и разгибательных поверхностях конечностей, щеках. Сыпь может быть уртикарной, пятнисто-папулезной, но все-таки визитной карточкой этого варианта является так называемая «линейная» сыпь, представляющая скопления мелких элементов сыпи в виде полосок длиной до 1 до 4 см. Для этого варианта ЮРА характерен высокий лейкоцитоз, тромбоцитоз, нейтрофиллез с палочкоядерным сдвигом до 15–20%. Скорость оседания эритроцитов (СОЭ) может достигать 80 мм/час [2].
Из висцеральных поражений при аллергосептическом варианте довольно часто развивается миокардит и миоперикардит, значительно утяжеляющий клиническую картину болезни.
В том случае, когда аллергосептический синдром протекает без поражения суставов, можно говорить о болезни Висслера–Фанкони без трансформации в ЮРА. Под нашим наблюдением находится ряд детей, у которых отмечался однократно или повторно аллергосептический синдром, иногда с преходящими экссудативными изменениями в суставах, однако рентгенологических признаков поражения суставов не отмечалось в течение длительного времени (более 10 лет). Проведенное иммуногенетическое обследование показало ряд особенностей иммуногенетических ассоциаций аллергосепсиса Висслера–Фанкони, отличных от аллергосептического варианта ЮРА [5]. Клинико-иммуногенетическое проспективное обследование больных с системными формами ЮРА позволяет предположить, что аллергосептический вариант ЮРА и аллергосепсис Висслера–Фанкони являются родственными, но не тождественными заболеваниями [2, 5].
Олигоартикулярный вариант ЮРА
По клиническим, иммунологическим и иммуногенетическим особенностям выделяется наблюдаемый преимущественно у девочек вариант ЮРА, начинающийся с моно- или олигоартрита в раннем детском возрасте.
Средний возраст начала заболевания составляет 2,5 года (от 6 месяцев до 6 лет), в дебюте у всех детей с этим вариантом ЮРА отмечается моно- или ассиметричный олигоартрит, преимущественно суставов ног. Чаще всего поражается коленный сустав. При олигоартикулярном начале помимо коленного сустава может поражаться голеностопный и/или лучезапястный суставы. В дальнейшем у 40% больных суставной синдром распространяется и принимает характер ограниченного полиартрита, у остальных пациентов продолжает рецидивировать в виде олигоартрита. Внесуставные проявления, такие как лихорадка, лимфаденопатия, гепатоспленомегалия нетипичны для данного варианта ЮРА. Наиболее частым и неблагоприятным внесуставным проявлением этого варианта ЮРА является иридоциклит. Развитие увеита при этой форме заболевания отмечается у 50% больных. Однако в течение последних 10 лет частота развития увеита у этих больных снизилась до 20–30%. Вероятно, активное проведение ранней иммуноподавляющей терапии, которое все шире стало использоваться у больных с олигоартикулярным вариантом ЮРА, предотвращает развитие увеита у большинства пациентов. Иммунологическими особенностями этого варианта являются отсутствие РФ и довольно частое (у 40%) выявление антинуклеарного фактора (АНФ) в невысоких титрах (1:40–1:80). Этот вариант олигоартрита часто называют «олигоартритом маленьких девочек», и, по мнению A. M. Prier, он не имеет аналогов у взрослых при ревматоидном артрите [1].
По нашим данным, согласующимся с результатами большинства иммуногенетических обследований аналогичных групп, приведенных в литературе, иммуногенетическими маркерами этого варианта ЮРА являются антигены HLA-А2 и HLA-DR5. Антиген гистосовместимости HLA-А2 выявлен у 80% больных с этим вариантом ЮРА. Даже при высокой частоте распространенности HLA-А2 в популяции, составляющей 49%, этот антиген гистосовместимости может рассматриваться как маркер олигоартрита маленьких девочек.
Среди антигенов гистосовместимости II класса наиболее высокой по нашим данным была частота HLA-DR5-антигена, который был выявлен у 80% больных этим вариантом ЮРА, при популяционной частоте этого антигена 30%.
Второй вариант олигоартрита характерен для мальчиков препубертатного, пубертатного возраста. Он характеризуется ассиметричным олигоартритом преимущественно суставов нижних конечностей, сопровождается поражением суставов свода стопы, болями в пятках (талалгиями), болями или болезненностью при пальпации в области прикрепления связок и сухожилий (энтезитами), вовлечением крестцово-подвздошных сочленений. Суставной синдром отличается торпидностью, прогрессирующим характером, особенно неблагоприятно протекает поражение тазобедренных суставов. Этот вариант по классификации ILAR может быть отнесен к энтезитному варианту ювенильного идиопатического артрита и, по сути, может рассматриваться как начальная стадия ювенильного спондилоартрита. Для этого варианта заболевания характерна ассоциация с HLA-В27, который выявляется у 50–80% пациентов этой группы. У 10% больных может развиваться передний увеит, сопровождающийся болью, покраснением глаз, светобоязнью [2, 5].
Полиартикулярный вариант ЮРА
Выделяют два субтипа полиартикулярного варианта ЮРА: серопозитивный по РФ и серонегативный по РФ.
Серопозитивный по ревматоидному фактору субтип ЮРА развивается преимущественно у девочек подросткового возраста, по своим клиническим, иммунологическим, иммуногенетическим особенностям он не отличается от серопозитивного по РФ полиартрита у взрослых. Клинически при этом субтипе ЮРА характерно симметричное поражение проксимальных межфаланговых, пястно-фаланговых, лучезапястных суставов, а также голеностопных и мелких суставов стопы. Больные отмечают утреннюю скованность, нарастающее ограничение подвижности суставов. Лабораторная активность умеренная, выявляется ревматоидный фактор. Иммуногенетическим маркером этого субтипа, как и при РА взрослых, является HLA-DR4. Кроме того, поражение суставов характеризуется быстрым развитием деструктивно-пролиферативных изменений.
Серонегативный по РФ субтип полиартрита также чаще встречается у девочек, характерно симметричное поражение крупных и мелких суставов с прогрессирующим течением заболевания. Течение артрита у большинства — относительно доброкачественное, однако у ряда пациентов могут развиваться тяжелые деструктивные изменения в суставах. Большинство ревматологов считает, что РФ-негативный полиартрит у детей соответствует РФ-негативному РА взрослых [2].
Для диагностики ЮРА чаще всего используют диагностические критерии Американской ревматологической ассоциации (АРА). К ним относятся следующие критерии:
- начало заболевания до достижения 16-летнего возраста;
- поражение одного и более суставов, характеризующееся припухлостью/выпотом либо имеющее как минимум два из следующих признаков: ограничение функции, болезненность при пальпации, повышение местной температуры;
- длительность суставных изменений не менее 6 недель;
- исключение других ревматических заболеваний.
Для постановки определенного диагноза необходимо наличие всех 4 признаков.
Диагностика ЮРА наиболее сложна в случае развития аллергосептического синдрома, когда суставной синдром отсутствует или слабо выражен, а в клинической картине доминирует гектическая лихорадка, сыпи, поражения внутренних органов. Так как этот симптомокомплекс присущ не только ревматоидным, но и другим заболеваниям, диагноз системной формы ЮРА ставится методом исключения следующих патологий:
- сепсис;
- инфекции (иерсиниоз, токсоплазмоз и др.);
- гематоонкологические заболевания, солидные опухоли;
- диффузные болезни соединительной ткани (системная красная волчанка, идиопатический дерматомиозит, системные васкулиты);
- периодическая болезнь;
- хронические заболевания кишечника (неспецифический язвенный колит, болезнь Крона).
В проведении дифференциальной диагностики необходимо использовать следующие методы:
- посевы биологических сред на флору с определением чувствительности;
- серологические методы для исключения инфекций;
- иммунологические исследования;
- биопсия костного мозга;
- компьютерная томография и/или магнитно-резонансная томография грудной, брюшной полостей, головного мозга;
- эндоскопические исследования;
- прокальцитониновый тест.
Особое значение в последние годы приобрел метод определения прокальцитонина, который позволяет дифференцировать воспалительные реакции, связанные с ЮРА, от воспалительных реакций, обусловленных бактериальной инфекцией. Известно, что при сепсисе и даже при локальном инфекционном процессе отмечается повышение уровня прокальцитонина, в то время как при ЮРА, даже в случае высокой клинико-лабораторной активности системной формы ЮРА, уровень прокальцитонина остается в норме [2].
Псориатический артрит
Псориатический артрит (ПсА) — это хроническое воспалительное заболевание суставов, которое развивается примерно у трети больных псориазом.
Классическими проявлениями псориаза у детей являются эритематозные папулы, покрытые серебристыми чешуйками, которые сливаются в бляшки различной формы. Чаще всего поражается кожа локтей, коленей, паховой области, волосистой части головы [6–8].
У большинства больных ПсА отсутствует четкая хронологическая зависимость между поражением кожи и суставов. Примерно у 75% пациентов поражение кожи предшествует развитию артрита, у 10–15% больных они возникают одновременно, однако еще в 10–15% случаев артрит развивается раньше псориаза [6–8].
У детей артрит в 50% случаев предшествует появлению псориаза. Однако даже при наличии у ребенка симптомов данного дерматоза, он обычно не столь явно выражен, как у взрослых, поэтому врачи нередко не замечают его [6–8].
Под нашим наблюдением находилось 28 пациентов с ПсА, у 29,4% детей заболевание началось с поражения кожи (поражение суставов у них развилось в среднем через 2,4 ± 0,3 года от начала заболевания), а у 70,6% пациентов в дебюте наблюдался суставной синдром (поражение кожи присоединилось в среднем через 4,5 ± 0,8 года), причем одна больная страдала артритом без кожных изменений в течение 8 лет.
ПсА может начинаться постепенно, исподволь (первые симптомы: повышенная утомляемость, миалгии, артралгии, энтезопатии, потеря массы тела). Приблизительно у трети детей в дебюте заболевания отмечается приступообразная резкая болезненность, отек и скованность в суставах, выраженная в утренние часы [6–8].
У подавляющего большинства (80%) больных ПсА чаще проявляется артритом дистальных, проксимальных межфаланговых суставов пальцев кистей, коленных суставов, реже — пястно- и плюснефаланговых, а также плечевых суставов [6–9].
По нашим сведениям, в дебюте заболевания у 17,6% пациентов отмечался аллергосептический синдром с лихорадкой, типичной сыпью, лимфоаденопатией, гепатолиенальным синдромом (по литературным данным, для ПсА нехарактерно вовлечение в процесс внутренних органов); у 11,8% — генерализованное поражение суставов, включая шейный отдел позвоночника, по типу синдрома Стилла; у 70,6% — олигоартикулярный асимметричный суставной синдром, причем процесс начинался с поражения голеностопных, коленных, проксимальных межфаланговых кистей и тазобедренных суставов.
Наиболее распространено деление ПсА на 5 классических форм [9]:
1) асимметричный олигоартрит;
2) артрит дистальных межфаланговых суставов;
3) симметричный ревматоидноподобный артрит;
4) мутилирующий артрит;
5) псориатический спондилит.
Эта классификация очень условна, формы заболевания нестабильны и могут со временем переходить одна в другую.
В 70% случаев ПсА проявляется асимметричным моно- или олигоартритом (асимметричность — характерная черта этого заболевания). Данной патологии свойственно также вовлечение в дебюте болезни так называемых суставов-исключений (межфалангового сустава I пальца и проксимального межфалангового — V пальца кисти). Особенностью ПсА является поражение всех суставов одного пальца кисти — аксиальный, или осевой, артрит. Нередко при этом наблюдается тендовагинит сухожилий сгибателей, что придает пораженному пальцу сосискообразный вид. Кожа над пораженными суставами, особенно пальцев кистей и стоп, нередко приобретает багровую или багрово-синюшную окраску [6–8].
В разгар заболевания (через 5–6 лет от начала болезни) у 41,2% пациентов диагностировался симметричный ревматоидоподобный артрит, у 23,5% — ассиметричный олигоартрит, у 23,5% — спондилоартрит с поражением периферических суставов (голеностопных, коленных, межфаланговых), у 11,8% — мутилирующий артрит.
Для постановки диагноза ПсА имеют значение асимметричный моно-, олигоартрит, особенно с поражением пальцев кистей или стоп, аксиальный артрит, вовлечение в дебюте болезни дистальных межфаланговых суставов или суставов-исключений, асимметричный сакроилеит. Определенные трудности диагностики возникают при отсутствии у больных кожного процесса. В этих случаях следует тщательно обследовать пациента с целью поиска даже минимальных проявлений псориаза [6, 7, 10].
Для постановки диагноза используются Ванкуверские диагностические критерии ювенильного ПсА (1989). Определенный ювенильный ПсА выявляется при наличии:
1) артрита и типичной псориатической сыпи;
2) артрита и хотя бы трех из следующих «малых» признаков:
— изменений ногтей (синдром «наперстка», онихолизис);
— псориаза у родственников 1-й или 2-й степени родства;
— псориазоподобной сыпи;
— дактилита.
Вероятный ювенильный ПсА определяется при наличии артрита и хотя бы двух из «малых» признаков.
Ювенильный анкилозирующий спондилоартрит
Ювенильный анкилозирующий спондилоартрит (ЮАС) — это заболевание с наследственной предрасположенностью, характеризующееся хроническим воспалительным процессом в суставах как периферических, так и в суставах осевого скелета, часто сочетающееся с энтезитами, серонегативностью по РФ и АНФ. Поскольку поражение суставов позвоночника может быть отсрочено на годы, обязательным критерием диагноза в детском возрасте является поражение крестцово-подвздошных сочленений [11].
Наиболее ранними проявлениями ЮАС является артрит одного или нескольких периферических суставов, обычно нижних конечностей, сочетающийся с энтезопатиями чаще пяточных костей. Системные проявления выражены минимально, но может иметь место субфебрильная лихорадка. Признаки поражения позвоночного столба обычно либо отсутствуют, либо слабо выражены и развиваются только во взрослом (редко в подростковом) возрасте, причем их прогрессирование происходит медленно и типичные рентгенологические изменения формируются позже обычного.
Чаще (до 80% случаев) в дебюте может отмечаться изолированный периферический артрит или изолированный энтезит. В 25% случаев ЮАС начинается с одновременного поражения периферических суставов и осевого скелета [12–14]. И очень редко с изолированного вовлечения в процесс осевого скелета или глаз.
Для артрита при ЮАС характерно преимущественное поражение суставов нижних конечностей; асимметричность суставного синдрома. Суставной синдром чаще представлен моно- или олигоартикулярным поражением, в редких случаях полиартритом. Для ЮАС характерно относительно доброкачественное течение с возможностью полного обратного развития и склонностью к длительным, в том числе многолетним, ремиссиям, недеструктивным характером артрита (за исключением тарзита и коксита). Периферический артрит при ЮАС часто сочетается с энтезитом [11].
Чаще всего артрит развивается в коленных, тазобедренных и голеностопных суставах и очень редко в суставах верхних конечностей (локтевых, лучезапястных, мелких суставов кистей). Кроме того, типичным считается при поражении мелких суставов вовлечение в процесс первых пальцев [11].
Наиболее приемлемыми для постановки диагноза являются диагностические критерии Гармиш–Партенкирхен (табл. 1).
Вероятному ЮАС соответствуют 2 основных критерия или 1–2 основных + 2 дополнительных критерия.
Определенному ЮАС соответствуют те же критерии + рентгенологически достоверный сакроилеит (двусторонний сакроилеит II стадии или односторонний сакроилеит не менее III стадии).
Реактивный артрит
Реактивный артрит (РеА) — это асептическое воспалительное заболевание суставов, развивающееся в ответ на внесуставную инфекцию, преимущественно кишечную и урогенитальную.
Синдром Рейтера
Классическим клиническим проявлением реактивного артрита является болезнь Рейтера или уретроокулосиновиальный синдром, который характеризуется классической триадой клинических симптомов — уретритом, коньюнктивитом, артритом [24–27]. Синдром Рейтера развивается в хронологической связи с перенесенной инфекцией мочеполового тракта или кишечника или на фоне персистирующей инфекции.
Синдром Рейтера, развивающийся на фоне хламидийной инфекции, у детей имеет ряд особенностей. В дебюте чаще всего отмечаются симптомы поражения урогенитального тракта (уретрит, баланит, баланопостит). В последующем присоединяются симптомы поражения глаз (чаще конъюнктивит) и суставов. Встречается так называемый неполный синдром Рейтера, при котором может отсутствовать поражение глаз или мочеполового тракта, но присутствует суставной синдром [15].
Поражение опорно-двигательного аппарата характеризуется развитием ограниченного асимметричного, моно-, олиго- и полиартрита. Отмечается преимущественное вовлечение в процесс суставов ног, с наиболее частым поражением коленных, голеностопных суставов, плюснефаланговых, проксимальных и дистальных межфаланговых суставов пальцев стоп. Артрит может начинаться остро, с выраженными экссудативными изменениями. У некоторых пациентов повышается температура, вплоть до фебрильных цифр.
Экссудативный артрит может протекать без боли, скованности, выраженного нарушения функции, с большим количеством синовиальной жидкости, непрерывно рецидивируя. Поражение суставов при этом характеризуется длительным отсутствием деструктивных изменений, несмотря на рецидивирующий синовит. Типичным для РеА является поражение первого пальца стопы, формирование «сосискообразной» деформации пальцев стоп (за счет выраженного отека и гиперемии пораженного пальца), развитие теносиновита и бурсита, развитие ахиллобурсита [15].
У ряда больных отмечается развитие энтезита и энтезопатий (боли и болезненность при пальпации в местах прикрепления сухожилий к костям), частые боли в пятках, боли, скованность, ограничение подвижности в шейном и поясничном отделе позвоночника. Эти клинические симптомы характерны для мальчиков подросткового возраста, с наличием HLA-B27. У этих детей имеется высокий риск формирования ювенильного спондилоартрита.
При затяжном (6–12 месяцев) или хроническом (более 12 месяцев) течении болезни характер суставного синдрома меняется. Увеличивается число пораженных суставов, артрит становится более симметричным, чаще вовлекаются суставы верхних конечностей и позвоночник.
Часто классические симптомы синдрома Рейтера хронологически не связаны между собой, что затрудняет диагностику.
Синдром Рейтера, ассоциированный с кишечной инфекцией
Синдром Рейтера, ассоциированный с кишечной инфекцией, протекает более остро, агрессивно, чем ассоциированный с хламидийной инфекцией. При постэнтероколитическом синдроме Рейтера обнаруживается более явная хронологическая связь с перенесенной кишечной инфекцией. Заболевание может протекать с выраженными симптомами интоксикации, лихорадкой, острым суставным синдромом, высокой лабораторной активностью. Все внесуставные проявления также носят более выраженный характер. При иерсиниозном РеА конъюнктивит может быть гнойным, тяжелым. У 1/3 больных может развиться острый иридоциклит, угрожающий слепотой. Уретрит характеризуется острым течением, поражения слизистых оболочек также более выражены, чем при хламидийном синдроме Рейтера [15].
Вероятный реактивный артрит (без отчетливых внесуставных поражений)
В ряде случаев РеА протекает без отчетливых внесуставных проявлений, относящихся к симптомокомплексу синдрома Рейтера (конъюнктивит, уретрит, кератодермия). В таких случаях ведущим в клинической картине является суставной синдром, который характеризуется преимущественным поражением суставов нижних конечностей, асимметричного характера. По количеству пораженных суставов преобладает моно-, олигоартрит. В целом характер и течение артрита аналогичны таковым при синдроме Рейтера. Типичным для РеА является поражение первого пальца стопы, формирование «сосискообразной» деформации пальцев стоп. У ряда больных возможно развитие энтезита и энтезопатий. Вне зависимости от наличия внесуставных проявлений у этих детей имеется высокий риск формирования ювенильного спондилоартрита.
В случае отсутствия полной клинической картины синдрома Рейтера, даже при характерном суставном синдроме диагноз РеА представляет значительные трудности. Наличие характерного моно-, олигоартрита, с преимущественным поражением суставов ног, выраженной экссудацией, связанного с перенесенной кишечной или урогенитальной инфекцией или с наличием серологических признаков перенесенной инфекции позволяет отнести заболевание к вероятному реактивному артриту [15].
Диагноз РеА ставится на основании диагностических критериев, принятых на III Международном совещании по реактивным артритам в Берлине в 1996 г. (табл. 2) [16].
Согласно этим критериям диагноз РеА можно поставить лишь в том случае, если у больного имеет место типичный периферический артрит, протекающий по типу асимметричного олигоартрита с преимущественным поражением суставов нижних конечностей [15].
Необходимо также наличие клинических признаков инфекции (диареи или уретрита), перенесенной за 2–4 недели до развития артрита. Лабораторное подтверждение в этом случае желательно, но не обязательно. При отсутствии клинических проявлений инфекции учитываются лабораторные данные, ее подтверждающие. Диагноз синдрома Рейтера или РеА ставится на основании данных о предшествующей инфекции, анализа особенностей клинической картины и данных лабораторных и инструментальных методов обследования и результатов этиологической диагностики [15].
Знание особенностей суставного синдрома при различных видах артритов у детей сокращает время постановки диагноза и позволяет проводить раннее начало антиревматической терапии, определить правильную тактику лечения и улучшить прогноз и качество жизни наших пациентов.
Литература
- Cassidi J. T., Petty R. E. Textbook of Pediatric Rheumatology. Toronto, W. B. Saunders Company. 819 p. 2002.
- Жолобова Е. С., Шахбазян И. Е., Улыбина О. В., Афонина Е. Ю. Ювенильный ревматоидный (идиопатический) артрит: руководство по детской ревматологии / Под ред. Н. А. Геппе, Н. С. Подчерняевой, Г. А. Лыскиной. М.: ГЭОТАР-Медиа, 2011. С. 162–244.
- Шахбазян И. Е. Детская ревматология: Рук-во для врачей / Под ред. А. А. Баранова, Л. К. Баженовой. М.: Медицина, 2002. С. 271–310.
- Prier A. M. Systemic forms of juvenile idiopathic arthritis: clinical course // Press Med. 2000. V. 29. P. 503–509.
- Жолобова Е. С. Роль наследственных (иммуногенетических) и средовых (инфекционных) факторов в развитии ювенильных артритов. Автореф. дисс. на соис. … д.м.н. М., 2005.
- Бунчук Н. В., Бадокин В. В., Коротаева Т. В. Псориатический артрит: ревматология национальное руководство/Под ред. Е. Л. Насонова, В. А. Насоновой. М.: ГЭОТАР-Медиа, 2008. С. 355–366.
- Бурдейный А. П. Псориатический артрит: ревматические болезни / Под ред. В. А. Насоновой, Н. В. Бунчук. М.: Медицина,1997. С. 314–324.
- Чебышева С. Н. Псориатический артрит: руководство по детской ревматологии / Под ред. Н. А. Геппе, Н. С. Подчерняевой, Г. А. Лыскиной. М.: ГЭОТАР-Медиа, 2011. С. 285–299.
- Moll J. M., Wright V. Psoriatic arthritis // Semin. Arthritis Rheum. 1973. № 3. Р. 55–78.
- Southwood T. R. Psoriatic arthritis // Textbook of pediatric rheumatology. Toronto: W. B. Saunders Company, 2002. Р. 345–354.
- Жолобова Е. С., Чебышева С. Н. Ювенильный спондилоартрит: руководство по детской ревматологии / Под ред. Н. А. Геппе, Н. С. Подчерняевой, Г. А. Лыскиной. М.: ГЭОТАР-Медиа, 2011. С. 245–264.
- Ross E., Petty R. E., Cassidi J. T. Juvenile Ankilosing Spondilitis. Textbook of Pediatric Rheumatology. Toronto, W. B. Saunders Company. 2002. 819 р.
- Никишина И. П. Ювенильный анкилозирующий спондилоартрит: кардиология и ревматология детского возраста / Под ред. Г. А. Самсыгиной, М. Ю. Щербаковой. М.: ИД Медпрактика-Мб, 2004.
- Burgos-Vargas R., Pacheco-Tena C., Vazquez-Mellado J. A short-term follow-up of enthesitis and arthritis in the active phase of juvenile onset spondyloarthropathies // Clin Exp Rheumatol. 2002, Sep-Oct; 20 (5): 727–731.
- Жолобова Е. С. Реактивный артрит: руководство по детской ревматологии / Под ред. Н. А. Геппе, Н. С. Подчерняевой, Г. А. Лыскиной. М.: ГЭОТАР-Медиа, 2011. С. 265–284.
- Kingsly G., Sieper J. Third Intenetional Workshop on Reactive Arthritis: an overview // Ann Rheum Dis. 1996. Vol. 55. P. 564–570.
Е. С. Жолобова, доктор медицинских наук, профессор
С. Н. Чебышева1, кандидат медицинских наук
А. В. Мелешкина, кандидат медицинских наук
ГБОУ ВПО Первый МГМУ им. И. М. Сеченова МЗ РФ, Москва
1 Контактная информация: bur@comtv.ru
Восстановление пароля
E-mail:
Авторизация
Регистрация
Книги — Ревматология
Учебный материал
Научно-популярное
Медицинская стандартизация
Последние добавленные статьи
- Дефицит витамина Д. Гиповитаминоз Д. Причины, клиника, диагностика дефицита витамина Д. Лечение дефицита витамина Д.
- Туберкулез и беременность. Клиника, диагностика туберкулеза у беременных. Профилактика туберкулеза у беременных.
- Риск внезапной сердечной смерти. Синдром Бругада. Кардиомиопатии. Шкала MADIT-II, шкала HCM Risk-SCD и другие.
- Риск инсульта – ишемического и геморрагического. Догоспитальная диагностика инсульта. Шкала LAMS, шкала RACE, шкала NIHSS, шкала ESRS и другие.
- Риск сердечной недостаточности. Риск и прогноз острой и хронической сердечной недостаточности. Шкала EFFECT, индекс IMPACT и другие.
Последние добавленные новости
- Более миллиарда жителей планеты могут потерять слух из-за использования наушников.
- Поздний ужин усиливает чувство голода на следующие 24 часа.
- 43 миллиона сотрудников — планетарный дефицит медицинских работников.
- Медикаментозная коррекция основных клинических проявлений ме
- Виды физической активности. Борьба со стрессовыми факторами.
- Немедикаментозное лечение метаболического синдрома. Диетотер
- Альдостерома левого надпочечника, первичный альдостеронизм (
- Острый гломерулонефрит с нефритическим синдромом, период нач
- Вторичный инсулинзависимый сахарный диабет тип II, тяжёлая ф
- ТЭЛА. Венозные тромбозы и эмболии. Диагностика и ведение пац
- Артериальная гипертония. Гипертонические кризы.
- Шейное сплетение
- Гогаева Л.Б., Мадаминова М.А., Базарбаева Ч.С., Нуралиев М.
- Крутов Г.М. — Лимфодренажный массаж в практике прикладной ки
- Котенко О.Н. — Нефрология. Клинические протоколы лечения.
Сайт является виртуальным хранилищем учебного материала медицинской направленности. Материалы, представленные на данном медицинском портале, были взяты из Интернета (находятся в свободном доступе), либо были присланы нам пользователями. Все материалы представлены исключительно в ознакомительных целях, права на материалы принадлежат их авторам и издательствам. Если Вы хотите пожаловаться на материалы сайта, пишите сюда
Наверх













